著者:Dylan Daniel 博士 - サイエンティフィック・ディベロップメント部門ディレクター
Date: July 2017
膵管腺癌(PDAC)は膵臓癌で最も多く、全体の 95% を占めています。2017年に米国で PDAC と診断される人の数は約 50,987 人、そして PDAC による死亡者数は約 40,936 人にのぼると見られ、PDAC は特に致死率の高い癌の一つと考えられています。米国では代謝拮抗剤と抗有糸分裂剤を併用したタキサン系化学療法が標準治療とされていますが、これまでのデータを見る限り、その効果は全生存期間が数週間長くなる程度でしかありません。このため、 アンメットメディカルニーズとして、膵臓癌への新たな治療アプローチが強く求められています。
膵臓癌の新しい治療アプローチは臨床アウトカムが芳しくない場合が多く、さらに最近はほかの癌において免疫系を利用した治療が奏効していることから、創薬研究の対象を免疫療法へ切り替えるケースが増えています。同系マウス膵臓癌細胞株の数は限られていますが、ラボコープは Immuno-Oncology への応用に向けて Pan02 PDAC モデルの特性を明らかにしました。Pan02 は 3-メチルコラントレンを同所投与した C57BL/6 マウスに由来し、標準的な化学療法剤の多くに対して反応を示しません。1 Pan02 は SMAD4 遺伝子の機能喪失変異を持ち、これはヒト膵臓癌の約 30% で不活性化変異に類似した機能を示します。2
平均および個々の増殖曲線
ラボコープは Pan02 を移植可能な断片化モデルとし、その増殖動態の平均値(図 1A)と個々の動物の増殖曲線(図 1B)を図示しました。Pan02 の平均腫瘍倍加時間は 6日で、ほとんどの同系マウス細胞株の腫瘍よりも長くなっています。増殖が遅ければ、腫瘍の増殖が安楽死の基準に達する前に免疫系を変更し、抗腫瘍活性を誘発することができるため、免疫療法において扱いやすいモデルと言えるかもしれません。
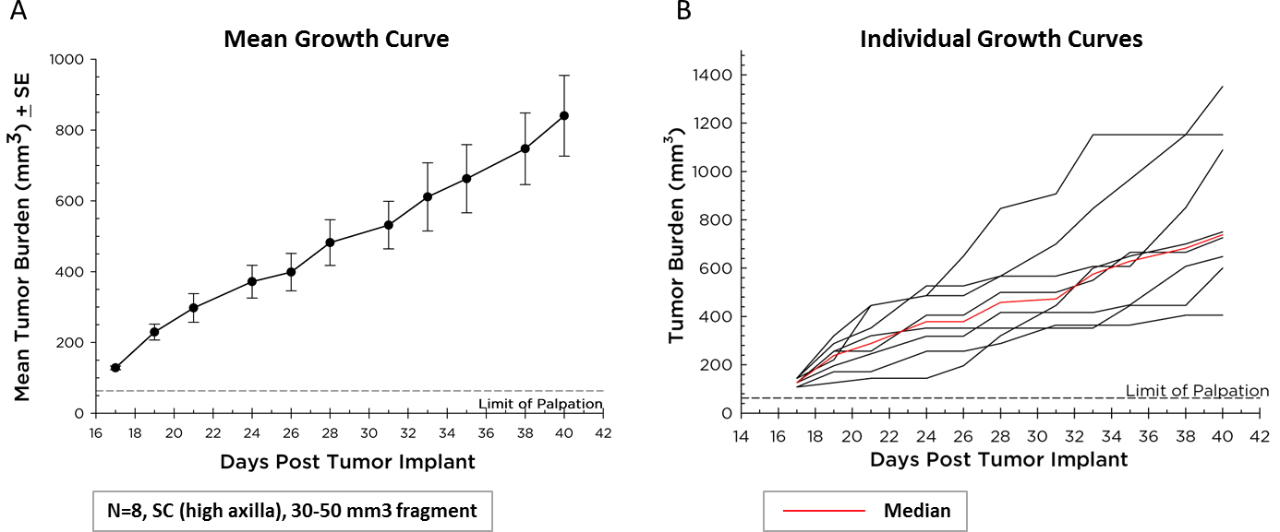
図 1 (A&B) - C57BL/6 マウスにおける Pan02 膵臓癌の増殖
抗 PD-1 および抗 CTLA-4 の有効性と生存率
現在、CTLA-4、PD-1、および PD-L1 に対する T細胞チェックポイント阻害剤抗体として承認されているものは、いずれも膵臓癌以外の疾患が対象となっています。コーヴァンスは、抗 CTLA-4(クローン 4F10)と抗 PD-1(クローン RMP1-14)を Pan02 モデルでそれぞれ単体使用した場合と併用した場合について試験を行いました。移植 3 日後に投薬を開始したところ、どの群でも平均群の腫瘍量に大きな変化は見られませんでした(図 2A)。多くの場合、免疫療法による活性が明らかになるのは治療中の動物のサブセット内に限られるため、個々の動物のプロットは反応者を検出するうえで有用です。しかし、個々の動物のプロットで検査薬による顕著な変化は見られず、対照群でも認められませんでした(図 2B)。また、増殖反応データから予想された通り、対照群と比較して治療群では生存率の改善が見られませんでした(図 3)。
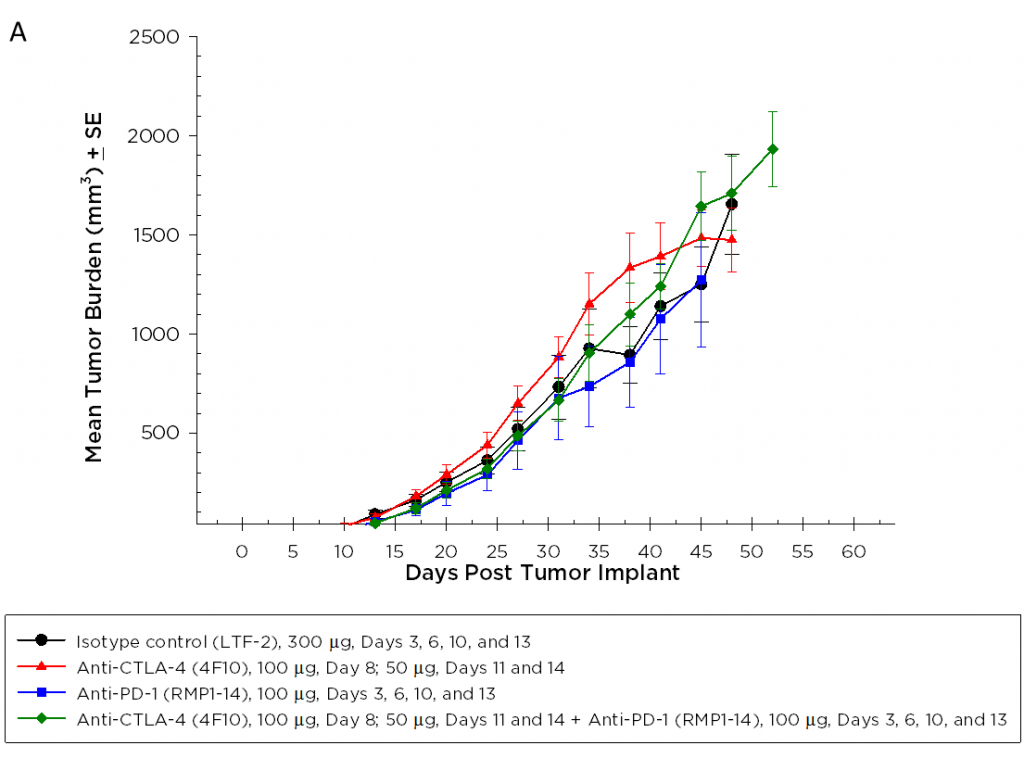
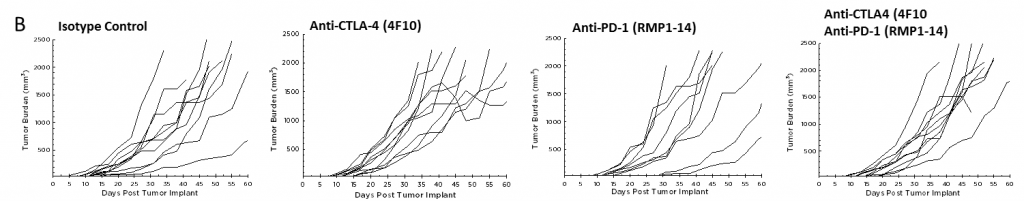
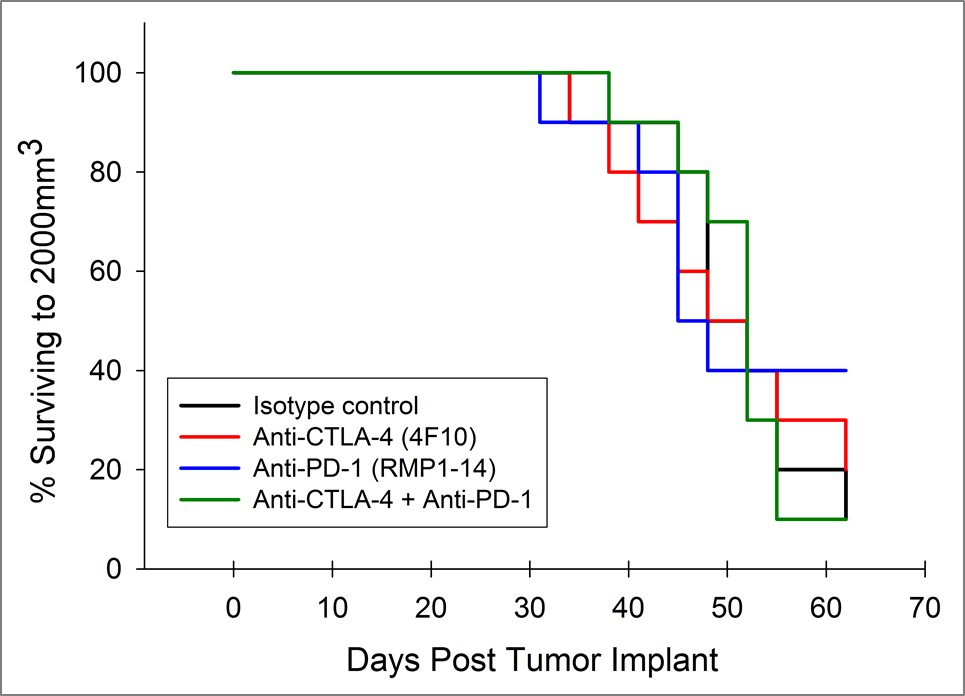
図 3:抗 PD-1 および抗 CTLA-4 による治療を受けた Pan02 膵臓腫瘍を有するマウスの生存率
免疫プロファイリング
チェックポイント阻害剤が、Pan02 腫瘍における免疫細胞浸潤に及ぼす影響を測定しました。図 4 は、全 CD45+ 白血球、CD4+ T 細胞、CD8+ T 細胞、制御性 T 細胞(Treg)、単球系骨髄由来免疫抑制細胞(M-MDSC)、および顆粒球性骨髄由来免疫抑制細胞(G-MDSC)の免疫プロファイルを示しています。
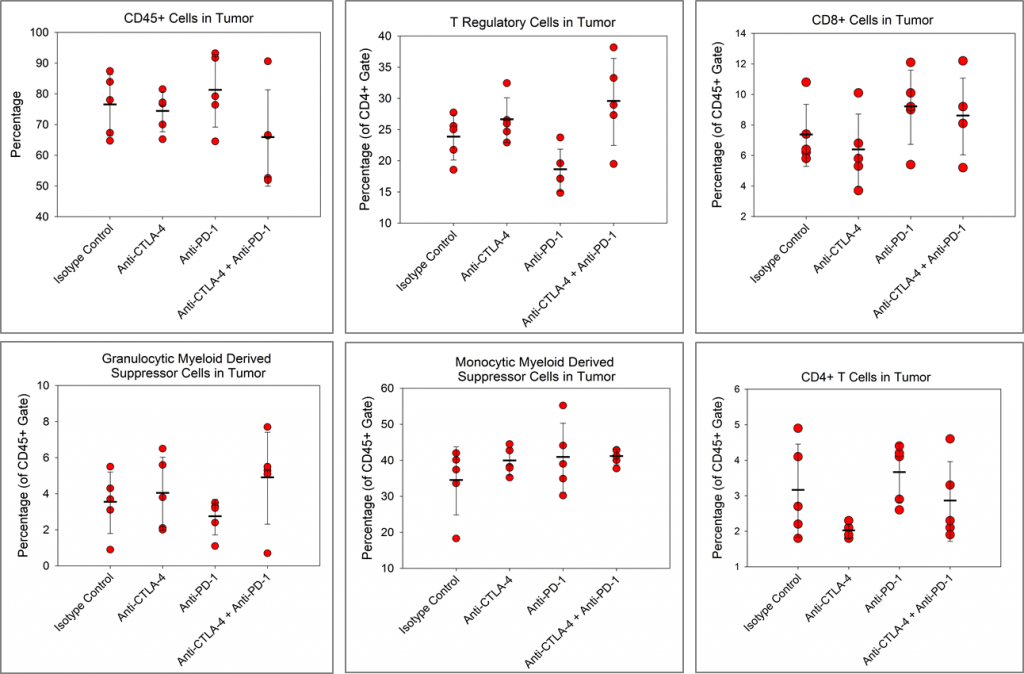
アイソタイプコントロールと比較すると、抗 CTLA-4 で治療した群では CD4+ T 細胞が減少、抗 PD-1 で治療した群では Treg が減少する傾向が見られましたが、その他の免疫変化は認められませんでした。チェックポイント阻害剤だけでは Pan02 モデルにおいて明らかな活性は見られませんが、複数の論文で、放射線 3 または共刺激アゴニスト抗 CD40 抗体による Pan02 腫瘍でのチェックポイント阻害剤の活性が報告されています。4 ここで重要となるのは、これらの研究において、抗 PD-L1 が抗 CD40 と放射線の両方と強く協同している点です。これは、Pan02 腫瘍がチェックポイント阻害剤単剤には反応しないものの、チェックポイント阻害剤によって併用パートナーの活性が促進される可能性を示唆しています。
Contact us to speak with one of our scientists to see how Pan02 or one of our other syngeneic models can be used for your next immuno-oncology study.
参照
2Wang Y et al., Genomic Sequencing of Key Genes in Mouse Pancreatic Cancer Cells. 2012. Curr Mol Med. Vol. 12(3): 331–341.
3Azad A et al., PD-L1 blockade enhances response of pancreatic ductal adenocarcinoma to radiotherapy. 2017. EMBO Mol Med. Vol 9: 167–180.
お問い合わせはこちら
お問い合わせ