著者:Erin Trachet | オンコロジー部門シニア科学顧問兼プロポーザルディベロップメント部門シニアマネージャー
Date: March 2018
先月のモデルスポットライトでも取り上げたとおり、肺癌は破壊的な病気で、米国、また世界における癌の死因の最多を占めるものです。1リサーチ コミュニティーは、引き続き肺癌研究に役立つ新しいモデルを探求しています。 現在ATCC(広く利用されている細胞レポジトリ)には100以上の異なったヒト由来の肺癌細胞株があります。
肺癌は広く蔓延しているため、新しいヒト細胞株を取得し特性化する機会は度々あります。サイエンティストたちは増殖を促す突然変異と増殖を抑制する突然変異を区別する技術において進歩を遂げています。この情報は肺癌の治療における新しい療法の開発に、非常に重要です。
Labcorp continues to investigate new and/or unconventional cell lines and understand their importance to our client's research.このモデルスポットライトではそのうち幾つかの細胞株について取り上げ、この分野の当社の専門知識をどのようにしてお客様の将来的な治療法開発における価値あるリソースとできるかを考えます。
NCI-H3122
NCI-H3122は、1981年に治療前の52歳男性の肺の原発細気管支肺胞上皮癌から派生したものです。この細胞株はEML4-ALK融合タンパク質(未分化リンパ腫キナーゼが棘皮動物微小管関連プロテイン質様4と融合したもの)を含み、最近になってNSCLC患者の4.5%、日本人のNSCLC(非小細胞肺がん)患者の~7%で識別されました。ALK遺伝子はその発癌性のため注目の的となっています。NCI-H3122 がEML4-ALKを含み、単剤ALK阻害剤に非常に敏感なため、その生存はよりALK依存の経路にかかっているようです。2前臨床のモデルとして、この細胞株はEGFR、またはNSCLC内の他の経路に依存しない新しいALK阻害剤の選考に適しています。 The model has been developed as a subcutaneous (SC) implant; however, we have also implanted this line intracranially to mimic the clinical setting where advanced NSCLC metastasizes to the brain. 皮下腫瘍増殖は着実で、動物個体間の変異性も最小でした。SC環境での腫瘍容積倍加期間は~7日間で、多くの場合マウスは、~750mm3の評価サイズにおよそ25日間で到達しました。NCI-H3122脳内インプラントの初期データは有望で、予備研究においての生着率は100、また体積評価によると腫瘍容積倍加期間は ~7日間で、これはSC増殖率とも一致した結果です(図表12を参照)。他の脳内モデルと同様、全体的な生存を定義するのに病的状態の観察(体重減と全体の臨床所見)が用いられています。この細胞株に関し、平均生存(死亡)期間は~35日間となっています(図表 2, 3, および4を参照)。
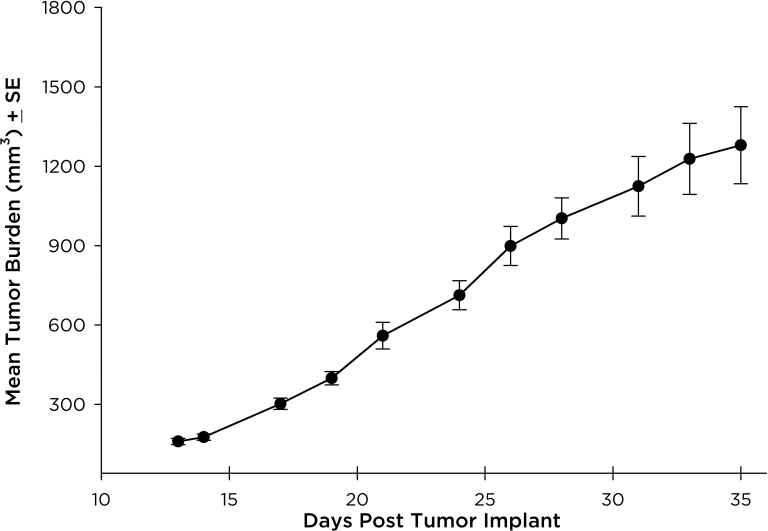
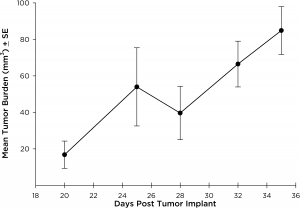
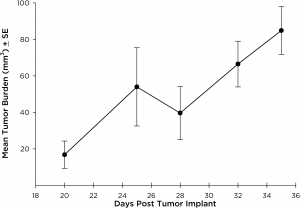
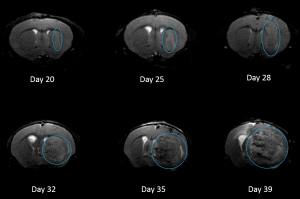
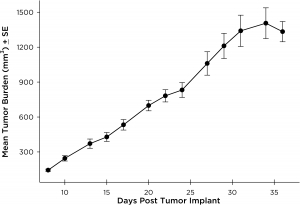
図 1:皮下 NCI-H3122 平均腫瘍組織量
図表2 : MRIに見る平均腫瘍増殖
図表3: NCI-H3122脳内移植後後の体重の変化(%)
Fig. 4: H3122-3160 Representative Image
NCI-H1703
NCI-H1703は54歳の喫煙白人男性のステージ1肺扁平上皮癌から派生しました。この細胞株はその血小板由来増殖因子α受容体(PDGFRa)増幅レベルの高さのため、リサーチコミュニティーに注目されています。 NCI-H1703 is one of very few NSCLC models that have this expression profile and are sensitive to sunitinib in vitro.臨床的に、PDGFRaを発現する肺癌患者はより浸潤性の高い腫瘍特性が見られ、思わしくない予後をもたらします。3したがって、このモデルは新しいVEGFのような血管新生標的や、細胞表面増殖径路から独立した新しいPDGFRa標的を評価するのに適しています。 The model is most commonly utilized following subcutaneous (SC) implant, however, we have also transfected this line with luciferase to allow for bioluminescence imaging to monitor disease progression following direct implant into the lung. Tumor growth is reliable following either SC or orthotopic (OT) lung implant. どちらの移植箇所でも動物個体間の変異性は最小限であり、腫瘍容積倍加時間も6日間(SC)および11日間(OT)です。 While the tumor growth rates are different for each implant site the mice typically reach evaluation size (~750mm3 or 1.0E+09 p/s) in approximately 30 days post implant (See Figures 5 [SC], 6, 7, and 8 [OT]).
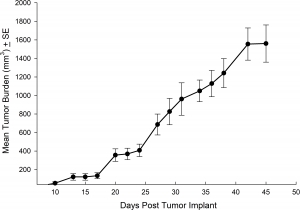
図表5: 皮下NCI-1703平均腫瘍負荷
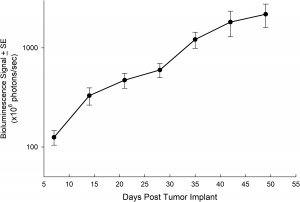
図表6: NCI-1703同所移植後の平均腫瘍負荷
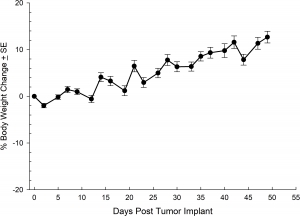
図表7: NCI-1703同所移植後の体重変化(%)
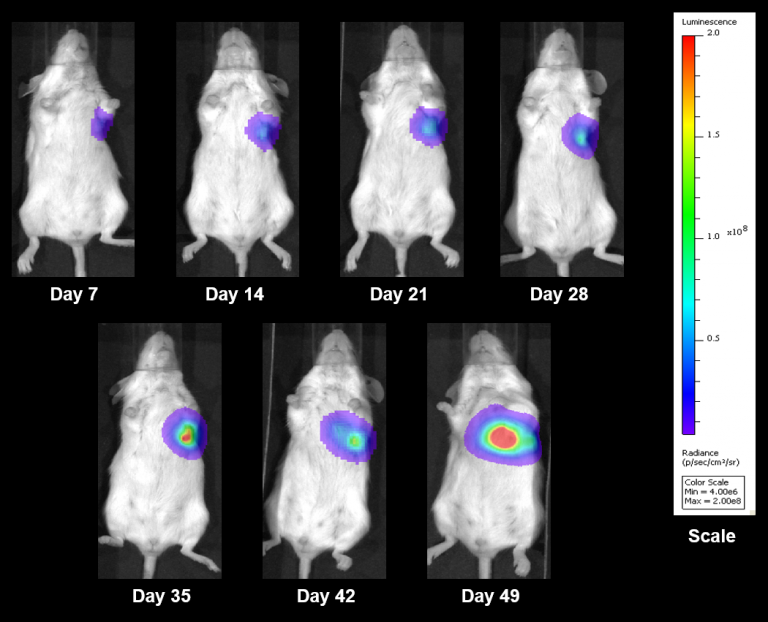
図表8: NCI-1703同所移植後の代表的BLI画像
PC-9
PC-9は、1989年に男性の肺腺癌患者より分離されました。PC-9は、ゲフィチニブおよび他のEGFRチロシンキナーゼ阻害剤に非常に敏感であることが報告されています。しかしながら、PC-9細胞はEGFR阻害剤に長期間曝露すると、T790M突然変異と耐性細胞株が発生する可能性も指摘されています。このモデルは次世代のEGFR阻害剤、または代替療法アプローチを評価するため、耐性バージョンを生成するにあたって有益です。 We have developed PC-9 as a subcutaneous model that demonstrates reliable growth with minimal animal-to-animal variability.腫瘍容積倍加期間は~7日間で、移植後、腫瘍は通常およそ28日で(~750mm3)の評価サイズに到達します(図表9)。
Please contact us if you are interested in discussing any of our human NSCLC models.
Investigate our full list of human xenograft models, including our extensive NSCLC Bank.
図表9: 皮下PC-9平均腫瘍負荷
参照
2EML4-ALK fusion gene and efficacy of an ALK kinase inhibitor in lung cancer. Jussi P. Koivunen, Craig Mermel, Kreshnik Zejnullahu, Carly Murphy, Eugene Lifshits,6 Alison J. Holmes, Hwan Geun Choi, Jhingook Kim, Derek Chiang, Roman Thomas, Jinseon Lee,9,10 William G. Richards, David J. Sugarbaker, Christopher Ducko, Neal Lindeman, J. Paul Marcoux, Jeffrey A. Engelman, Nathanael S. Gray, Charles Lee, Matthew Meyerson, and Pasi A. Jänne. Clin Cancer Res. 2008 Jul 1; 14(13): 4275–4283.
3Stromal Platelet-Derived Growth Factor Receptor α (PDGFRα) Provides a Therapeutic Target Independent of Tumor Cell PDGFRα Expression in Lung Cancer Xenografts. David E. Gerber, Puja Gupta, Michael T. Dellinger, Jason E. Toombs, Michael Peyton, Inga Duignan, Jennifer Malaby, Timothy Bailey, Colleen Burns, Rolf A. Brekken and Nick Loizos Molecular Cancer Therapeutics 10.1158/1535-7163.MCT-12-0431 Published November 2012.
お問い合わせはこちら
お問い合わせ