Date: February 2020
免疫不全マウスはデザイン上適応免疫がないため、ヒト腫瘍の移植や増殖のサポートに理想的な宿主です。免疫不全マウスを用いた前臨床異種移植モデルは、この機能的な免疫細胞が欠如していることから免疫療法の調査に限定されています。この「注目のモデル」では、ヒト T リンパ球細胞が免疫不全マウスで増殖し、腫瘍異種移植片の増殖を促すことについて説明します。
ヒト抹消居血単核細胞(hPBMC : Peripheral Blood Mononuclear Cell)を生着した NOD-scid IL2Rγnull (NSG)マウスは、異種移植モデルで利用され、ヒト T リンパ球上のエピトープをターゲットにした免疫チェックポイント阻害薬の有効性や薬力学の評価に成功しています1。 従来の異種移植モデルと違いこのモデルはユニークです。それは、機能性のあるヒト T 細胞が、マウスの腫瘍上のヒトエピトープをターゲットにし、臨床的な重要性を直接解釈することができるからです。NSG マウスは、樹状細胞とマクロファージ細胞の母集団が不足し、ある 2 つの特化した突然変異を持っているためリンパ球が著しく低下します。Pkrdc 変異は B 細胞および T 細胞を欠損させる DNA 修復の側面を無効にし、IL2Rγ の欠失により NK 細胞の成熟を阻害します2。この欠損の組み合わせによって hPBMC の生着が可能になり、NSG マウスのヒト T リンパ球の増殖が可能になります。
hPBMC が生着した NSG マウスに関しては注意すべき点があり、ヒトドナーと腫瘍モデルの選択前に検討しなければなりません。まず、ヒト免疫細胞をマウスに移植すると、移植片対宿主病(GvHD:Graft Versus Host Disease)と一致する T 細胞媒介毒性をもたらします。これは、ヒトリンパ球がマウスの組織を攻撃し、治療濃度域に限度が生じることになります3。次に、生着効率、存在する細胞の型、および活動は、ヒトのドナー源によって可変することが観察されています4。最後に、ヒト腫瘍異種移植片に hPBMC 拒絶のケースが観察されました(データ表示なし)。決定的な有効性試験を開始する前にドナー源と選択した腫瘍モデルを使用してこれらのパラメータを評価することは、トランスレーショナルな非臨床プログラムの成功にとって重要です。
実験デザイン
この研究の目的は、皮下ヒト腫瘍異種移植をした NSG マウスに移植された hPBMC からのヒト T リンパ球の生着を評価することです。動物のケアと使用は、AALAC 認可施設での「Guide for the Care and Use of Laboratory Animals」(実験動物の管理と使用に関する指針)に従って実施されました。皮下 MiaPaCa-2 ヒト膵管腺癌を移植した NSG マウス(ジャクソン研究所、米国メイン州バーハーバー 株 #0005557)は、4人の異なる正常な健康体ドナー(Hemacare、米国カリフォルニア州ロサンゼルス)からの hPBMCs を静脈内移植しました。腫瘍の増殖、体重、および GvHD と類似した特性の評価を実施しました。ヒトリンパ球マーカーのフローサイトメトリー分析のために全血を採取し、CD4+ および CD8+ 細胞を含めた CD45+ 細胞のドナーの生着を hPBMC を移植済みの状態で 14 日、 28 日と 42 日目に確認しました(図 1)。
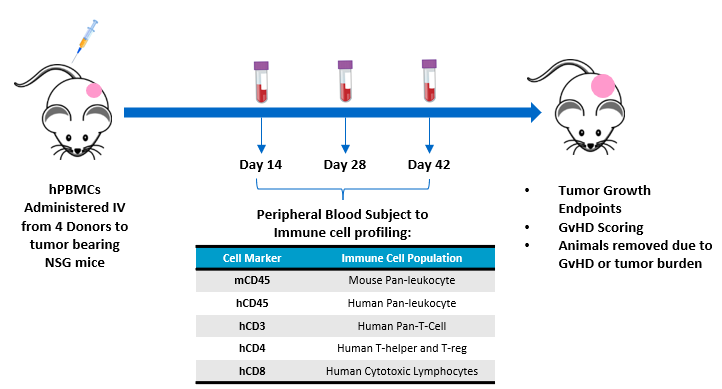
図 1 - MiaPaca-2 腫瘍を移植した NSG マウスの hPBMC 生着を評価する実験デザイン
腫瘍の増殖、体重、疾患の進行
無治療対照動物の MiaPaCa-2 腫瘍倍加時間(Td)は、9.1 日でした。hPBMCs を移植した動物の Td は、それぞれのドナーグループにおいて 8.7 日から 11.6 日の範囲でした。移植後 30 日を超えて hPBMC を移植した個体全体で増殖に変動性が観察されました。1000mm3 前の腫瘍の増殖は、hPBMC 生着による影響は見られませんでした(図 2)。これらの結果からも、使用したいずれのドナーも、1000mm3 の評価サイズまでの時間(TES:time to evaluation size)を使った MiaPaCa2 の有効性研究に適してると言えるでしょう。
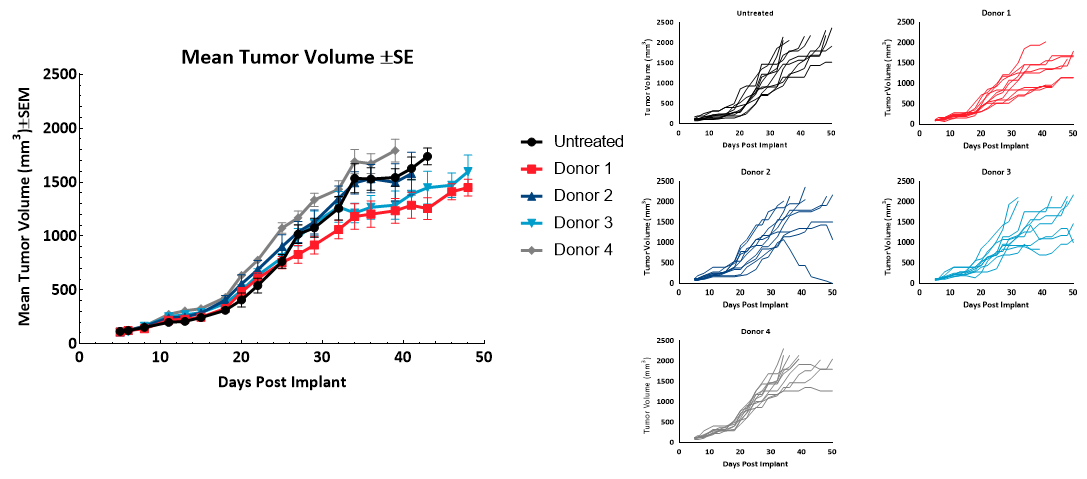
図 2 - hPBMC 移植後の MiaPaCa2 皮下腫瘍(n=10)の増殖
GvHD の初期症状は体重と臨床観察で監視されました。この研究は理学的には立証されていませんが、このモデルで観察された症状は、疾患と強い相関性を表しています5。基準値の 10% を超える体重減少(図 3)、毛並みのごわつき、猫背、皮膚障害、下痢等の症状のすべてが現れた場合、またはそれらいくつかの症状が重篤であった場合、動物はこの研究から省きました。hPBMC 注入 32 日経過後、各グループの半数以上の動物で臨床兆候が観察されました。GvHD 症状で省かれていない動物は、2000mm3を超過した腫瘍組織量もしくは、研究終了のために省かれました。
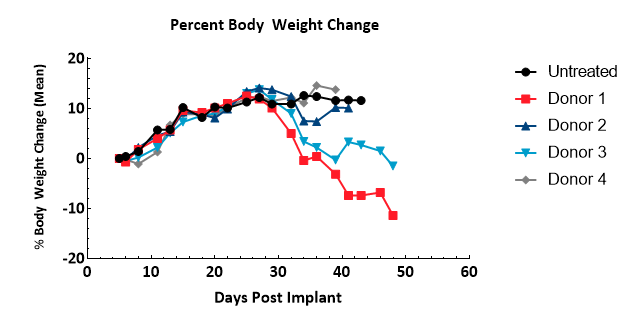
図 3 - hPBMC 移植後の体重変化
ヒトリンパ球の生着と残留
NSG マウスの末梢血にあるヒト免疫細胞マーカーの免疫表現型解析で hPBMC を移植後、14 日目、 28 日目、42 日目にその生着率を測定したところ、mCD45(マウス汎白血球)、hCD45(ヒト汎白血球)、hCD3(汎 T 細胞)、hCD4(T ヘルパーおよび T レグ)、hCD8(細胞傷害性リンパ球)が フローサイトメトリーで検出されました(図 4)。
GvHD の初期症状は体重と臨床観察で監視されました。この研究は理学的には立証されていませんが、このモデルで観察された症状は、疾患と強い相関性を表しています5。基準値の 10% を超える体重減少(図 3)、毛並みのごわつき、猫背、皮膚障害、下痢等の症状のすべてが現れた場合、またはそれらいくつかの症状が重篤であった場合、動物はこの研究から省きました。hPBMC 注入 32 日経過後、各グループの半数以上の動物で臨床兆候が観察されました。GvHD 症状で省かれていない動物は、2000mm3を超過した腫瘍組織量もしくは、研究終了のために省かれました。
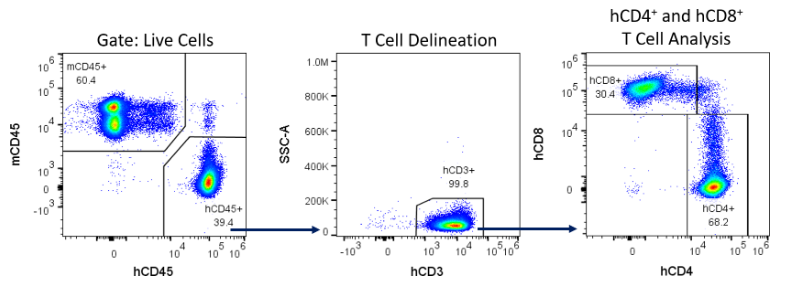
図 4 - hPBMC で再構成された NSG マウスにおけるヒト免疫細胞の検出のためのゲーティング戦略例
hCD45+ 割合は、合計生細胞数の hCD45+ 細胞の割合として計算され(全血の絶対細胞数 /µL に基づく)、hPBMC 生着率の指標として使われています。全血中の %hCD45+ 細胞がすべてのドナーにおいて経時的に検出されたことを発見しました(図 5)。しかし、ドナー 2 と 4 は hPBMC 移植後 42 日目の生着率が高くないドナー 1 と 3 と比較して、固体ベースで hCD45 細胞が著しく増殖しました。 Animals across all groups achieved %hCD45 engraftment levels 28 days post hPBMC administration that is consistent with published literature on the model6.
NSG マウスに hPBMC を移植すると、MiaPaCa-2 腫瘍増殖の影響が最小限であったマウスにヒト T 細胞が残留しました。このモデルは、直接的な臨床的意義のある抗腫瘍活性に直結したヒト T リンパ球を活用する新薬効果の検証において、強力な前臨床プラットフォームとなります。今後の研究により、hPBMC で再構成された NSG マウスへのヒト腫瘍異種移植に対する、FDA 承認を受けた免疫療法の有効性が実証されるでしょう。
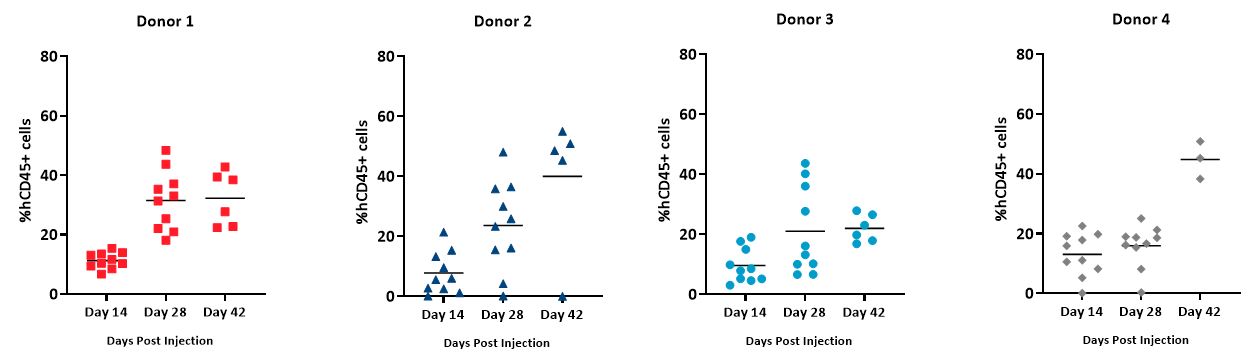
図 5 - hPBMC 移植後の NSG マウスの全血から検出された hCD45+ 細胞の生着範囲
Please contact our preclinical oncology scientists to see how hPBMC engrafted NSG mice can be used for your next translational immuno-oncology study.
参照
お問い合わせはこちら
お問い合わせ