Date: October 2018
Hepatocellular carcinoma (HCC) is an aggressive malignancy which has gradually increased in incidence to affect one million people worldwide and is currently the third leading cause of cancer related deaths in the world.[1,2] The prevalence of HCC is highest in Asia and Africa due to high endemicity of hepatitis B and C viruses which strongly predispose to the development of chronic liver disease and subsequent HCC.[1]
In the Western population, hepatitis C, alcoholic cirrhosis, and non-alcoholic steatohepatitis (NASH) are the main underlying causes. 早期段階のHCC治療の選択肢としては、外科的切除、肝臓移植、化学療法および放射線塞栓療法、そしてラジオ波焼灼療法なども候補に挙げられますが、進行したHCCには、標的療法(ソラフェニブとレゴラフェ二ブ)、放射線そして化学療法(ドキソルビシン、5-FU、またシスプラチン)が一般的です。3現在、切除不能なケースや、進行したHCCの単一または併用免疫療法、モノクローナル抗体または腫瘍溶解性ウイルス療法に関する様々な治験が進行中です。1-4このような療法によって腫瘍の縮小や生存率の向上という結果を見てはいるものの、肝炎、肝硬変または非アルコール性脂肪肝疾患(NAFLD)などの持病によっては結果が左右され、治癒には至らないのが現状です。したがって、より良い治療法の選択肢に対するニーズは、常に増え続けていると言えます。 To evaluate novel therapies in a preclinical platform, Labcorp has established the syngeneic HCC model Hepa 1-6.
Hepa1-6は、C57L/Jマウスにおいて自然に発生したBW7756肝細胞腫瘍に由来するマウス肝細胞癌で、化学的に転移あるいは誘発させたほとんどの入手可能な肝細胞癌モデル(BNL、A.7R.1、MH-129、MH134そしてMH-22A)系統とは対照的です。免疫応答性のあるマウスで確立されたHepa1-6腫瘍モデルは、免疫療法の前臨床試験のための、臨床的に意義のあるモデルを代表しています。
In this model spotlight we present in vivo data on Hepa 1-6 tumor model growth kinetics; along with response to checkpoint inhibitors alone or in combination with focal radiation. 当社ではこのモデルの親C57LJ細胞株(メイン州バーハーバーにあるジャクソン研究所で入手できる限定的な数)、およびより入手しやすい組織適合C57BL/6系統を検証しました。
Hepa1-6増殖パラメータ
皮下インプラント後の増殖キネティクスは、どちらのマウス系統にもこのモデルが確立することを示しています。 腫瘍は、平均~5-6日間で特に有害な体重の変化もなく倍増しています(データ未掲載)。この安定した増殖ペースは、抗腫瘍反応を評価するのに3週間の治療期間猶予を可能にします。
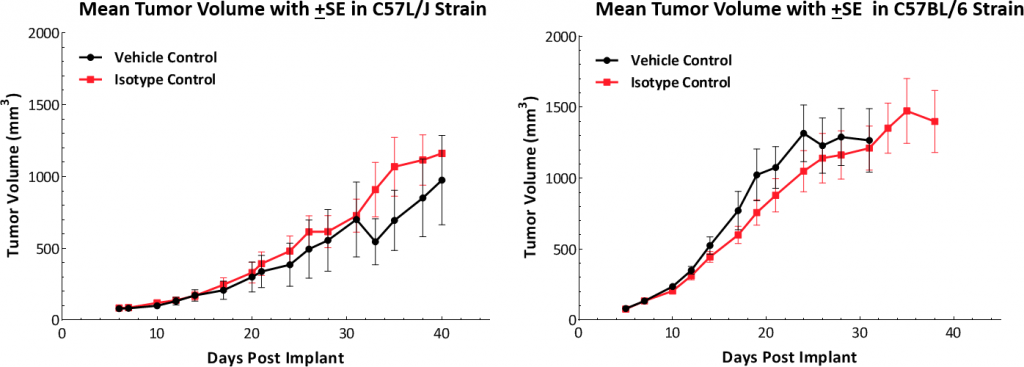
図表1:C57/JおよびC57BL/6マウスにおけるHepa1-6 腫瘍の増殖キネティクス
Hepa1-6腫瘍免疫細胞プロフィール
Hepa 1-6腫瘍の免疫プロフィールを理解するために、フローサイトメトリーによってベースライン免疫構成が分析され、図表2に表示されています。免疫プロフィールはC57L/J 系統に~750-1000mmの大きさまで増殖した5つの非治療Hepa 1-6腫瘍3から確立されています。 腫瘍は比較的高いCD45+細胞集団( 骨髄系の個体数は主にG(顆粒球型)-MDSC(平均~30%)、次にM(単球型)-MDSC(平均~11%)となっています。腫瘍内の微小環境で起こるCD8+T細胞浸潤は、免疫学的に応答性がある、あるいは「暖かい」腫瘍モデルを示唆しています。
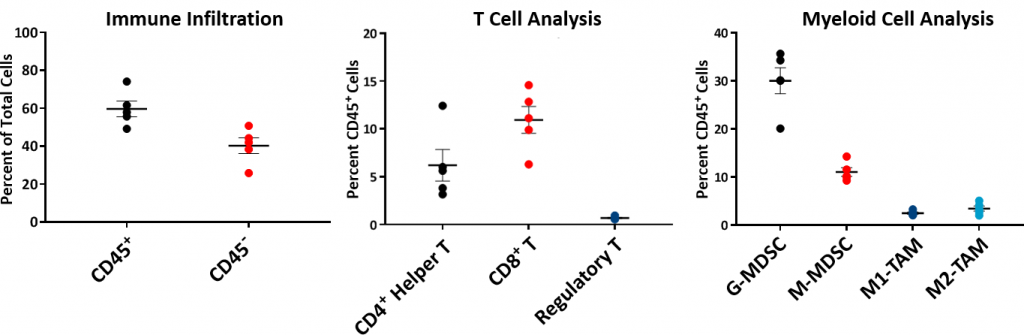
図表2:C57L/J マウスにおけるベースラインHepa1-6 腫瘍の免疫プロフィール
チェックポイント阻害剤に対するHepa1-6の反応
チェックポイント阻害抗体(抗mPD-1, 抗mPD-L1, および 抗mCTLA-4)によって治療された担腫瘍(平均腫瘍サイズ~100mm3)C57BL/6 マウスにおいて、免疫調整剤に対するHepa 1-6の 反応が評価されました。コントロール、媒介物(PBS)およびアイソタイプ(ラット IgG2b クローン LTF-2)は、同程度の増殖キネティクスを示しました(図表1)。単剤のチェックポイント阻害剤である抗mPD-1 また抗mCTLA-4は強い反応を誘発し、腫瘍の完全な退縮(CR)および無腫瘍生存率(TFS)が100%という結果を導き出しました。抗mPD-L1療法は動物のサブセットにおいても良好な反応を示し、CRまた5/10TFS(図表3)という結果に至りました。対照群の動物に関しては、チェックポイント阻害抗体による治療は、著しい体重の変化と関連付けることはできませんでした。免疫療法に対しての反応は、免疫学的に「熱い」Hepa 1-6 腫瘍の特徴を強く裏付けています。
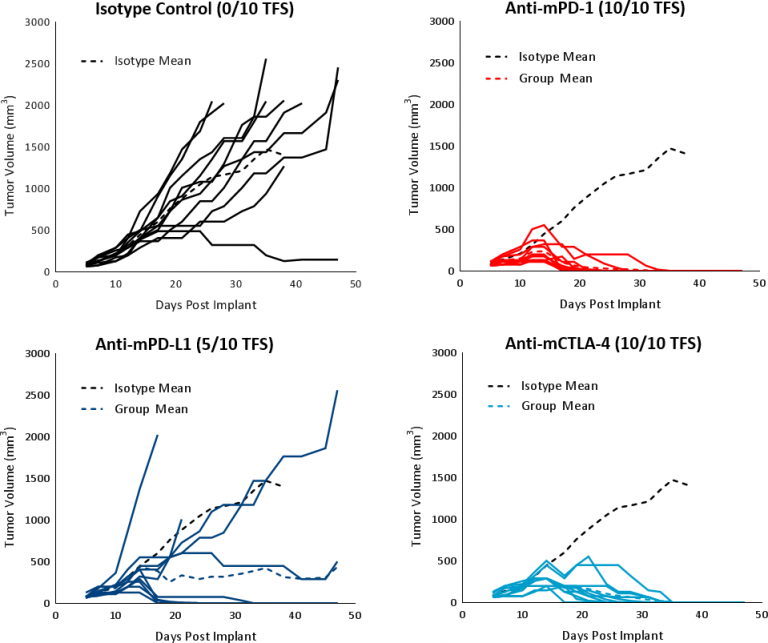
図表3:C57BL/6 マウスへのチェックポイント阻害剤に対するHepa 1-6腫瘍の反応
焦点放射線に対する反応
臨床的に言って、非転移性の肝細胞癌(HCC)を抱える患者様は、放射線療法(RT)又は体幹部定位放射線治療(SBRT)など一つかそれ以上の肝臓をターゲットにした治療(LDT)を受けることになります。5放射線療法は腫瘍を縮小、またはその微小環境を腫瘍抑制環境に変化させることができます。放射線療法に対するHepa 1-6腫瘍の反応を検証するため、標的領域に焦点ビーム放射線を照射するのに、 小動物放射線研究プラットフォーム(SARRP; Xstrahl)を用いました。 C57BL/6 マウスの Hepa 1-6皮下腫瘍に、5および10Gyの焦点放射線が使用されました。>治療は放射線投与の量に比例して>20 日間の腫瘍増殖遅延(TGD)、そして無腫瘍生存率(それぞれ2/10および810)という結果を示しました(図表4)。5Gyの照射で、寿命の延長を含む中程度の単剤療法反応が得られたことから、今後の併用研究が推奨されます。
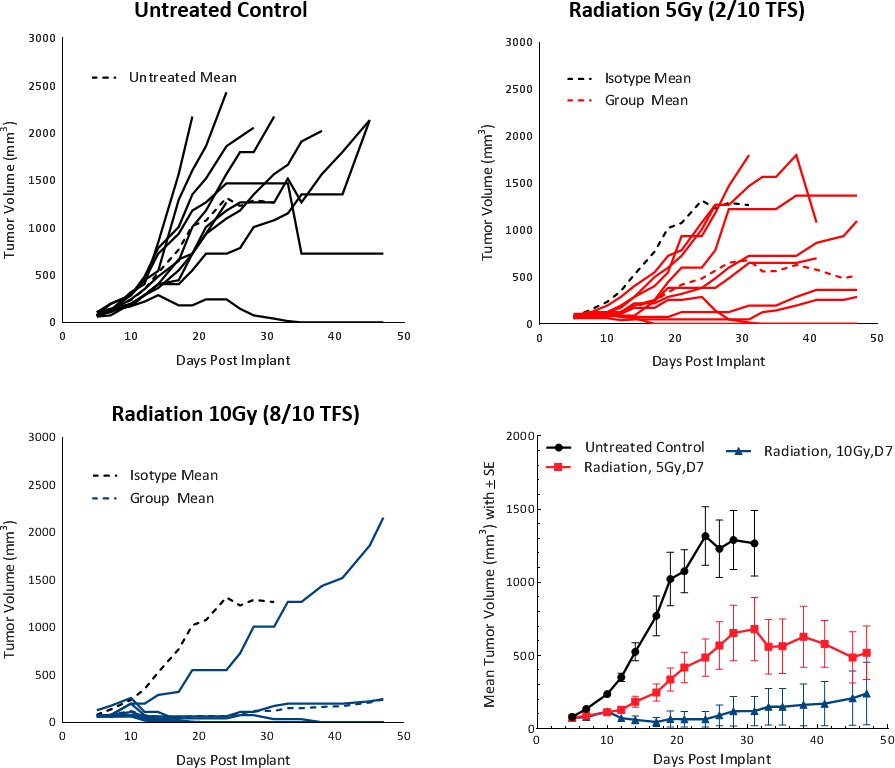
図表4:C57BL/6 マウスへの放射線療法に対するHepa1-6 腫瘍の反応
ソラフェニブに対するHepa1-6の反応
Rafキナーゼ、Src、血管内皮細胞増殖因子(VEGF)また血小板由来成長因子(PDGF)受容体をブロックする多標的チロシンキナーゼ阻害剤で、肝細胞癌(HCC)患者に最初の治療として使用されるソラフェニブがHepa 1-6腫瘍で試験されました。この治療は、25.4 日間の腫瘍増殖遅延期間、そして無腫瘍生存(TFS)ケースは無かったものの、全体的な生存率の延長という結果を見ました(図表5)。こうした結果は、統制群の7.9か月から治療群の10.7か月へと全体平均生存率の延長を見た、部分的反応の臨床研究結果とほぼ同等の数値を残しています。[1]
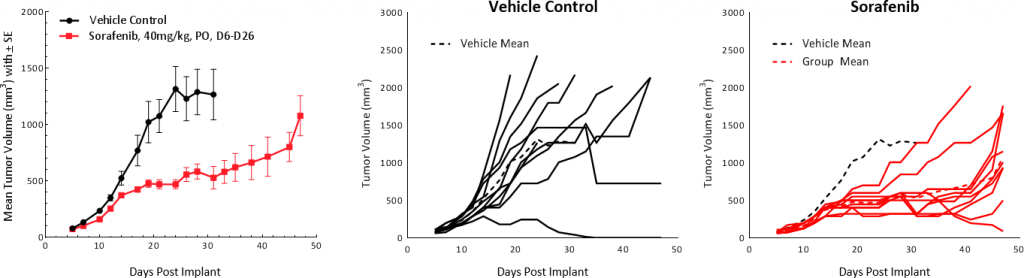
図表5:C57BL/6マウスへのソラフェニブ投与療法に対するHepa1-6 腫瘍の反応
こうした暫定データは、肝細胞癌(HCC)のHepa 1-6モデルが望ましい免疫プロフィールを有していること、そして強固な前臨床immuno-oncologyモデルとして採用できることを示唆しています。 当社のデータは単剤療法、放射線との併用、少分子、標準治療、また他の新興治療法として免疫療法の治療薬を検証するのに、このモデルが使用に耐えうることを示しています。
Please contact us to speak with our scientists about how Hepa 1-6 can be used for your next immuno-oncology study.
参照
[1]Medavaram, S and Zhang Y, 2018. 「進行した肝細胞癌に対する発展途上の治療法 」 Exp Hematol Oncol 7:17.
[2]Llovet JM, Montal R, Sia D and Finn RS, 2018. 「肝細胞癌に対する分子療法とプレシジョンメディシン」 Nat Rev Clin Oncol. doi: 10.1038/s41571-018-0073-4.(印刷前の電子出版) PMID:30061739.
[3]Pinter M & Peck-Radosvljevic M. 2018. 総説論文:「肝細胞癌の全身療法 2018」 Aliment Pharmacol Thera、7月 23. doi: 10.1111/apt.14913. (印刷前の電子出版)総説. PMID: 30039640.
[4]Waidmann O. 2018. 「肝細胞癌に対する免疫療法の最近の展開」 Expert Opin Biol Ther. 8月;18(8):905-910.
お問い合わせはこちら
お問い合わせ